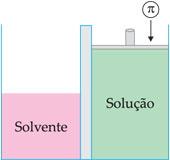
Pressão osmótica é a pressão que se deveria aplicar sobre a solução para impedir a passagem do solvente através da membrana semipermeável. A pressão osmótica é representada pela letra grega p. Essa pressão é equivalente à pressão exercida pelo solvente na passagem através da membrana.
Importante saber:Osmoscopia é a medida da pressão osmótica, que pode ser medida por aparelhos chamados osmômetros.Soluções isotônicas são soluções de mesma pressão osmótica. Uma solução será hipotônica em relação à outra, quando tiver menor pressão osmótica; e será hipertônica quando tiver maior pressão osmótica.
*Quanto maior for a diferença de concentração entre as duas soluções, maior será o fenômeno da osmose e consequentemente maior será a pressão osmótica capaz de impedir que a solução hipertônica seja diluída.
Existem algumas fórmulas em base as leis de Van´t Holf, mas nesta postagem nós nao colocaremos ela mas somente os seus seguintes conceitos:1a) A pressão osmótica é diretamente proporcional à temperatura absoluta da solução.2a) A pressão osmótica é diretamente proporcional à concentração molar da solução.
reprise sobre o que foi visto até agora..
| EFEITO COLIGATIVO | PROPRIEDADE COLIGATIVA |
| Diminuição da pressão de vapor | Tonoscopia |
| Aumento do Ponto de Ebulição | Ebulioscopia |
| Diminuição do Ponto de Congelamento | Crioscopia |
| Aumento da Pressão Osmótica | Osmoscopia |
Obrigado por lerem..próximas postagens sobre química em breve...XoXo Taís e Rafa.
Nenhum comentário:
Postar um comentário